2025-07-04 13:46:23来源:鼎泰集团TriApex浏览量:1823
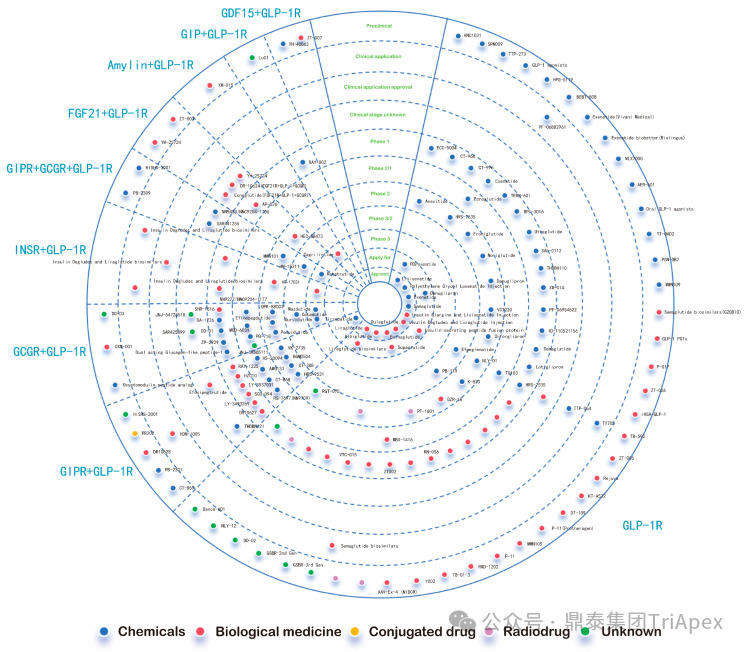
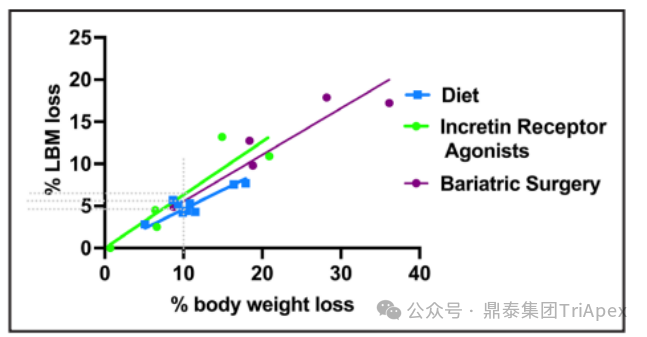
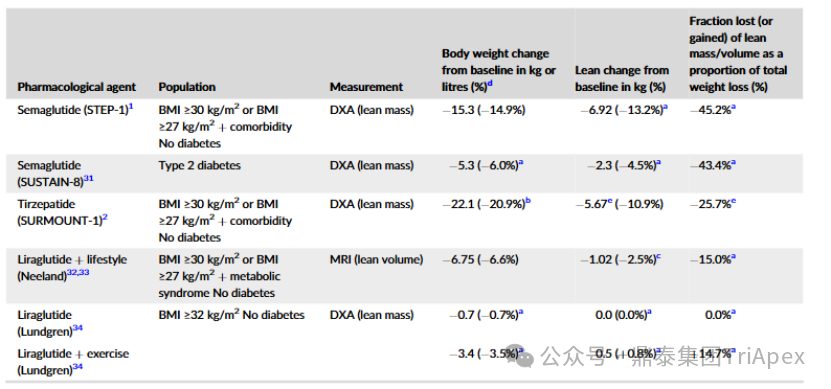
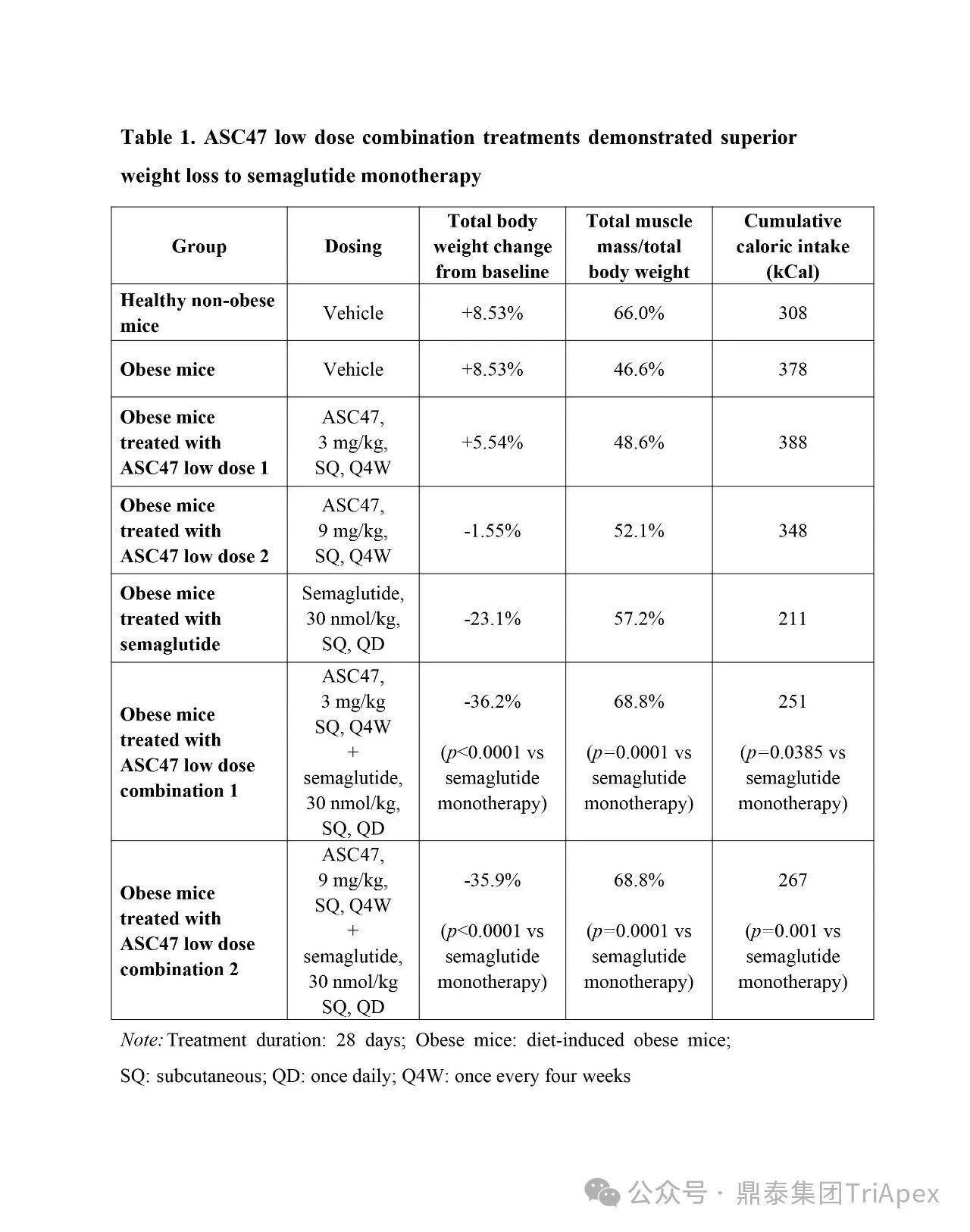
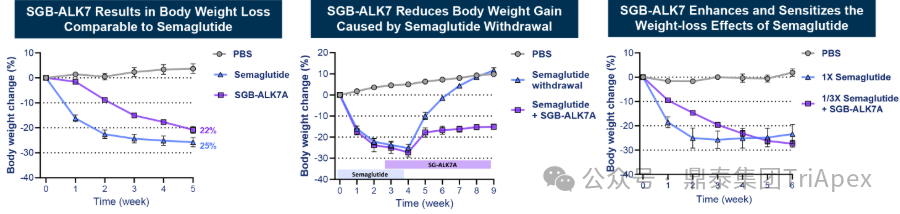
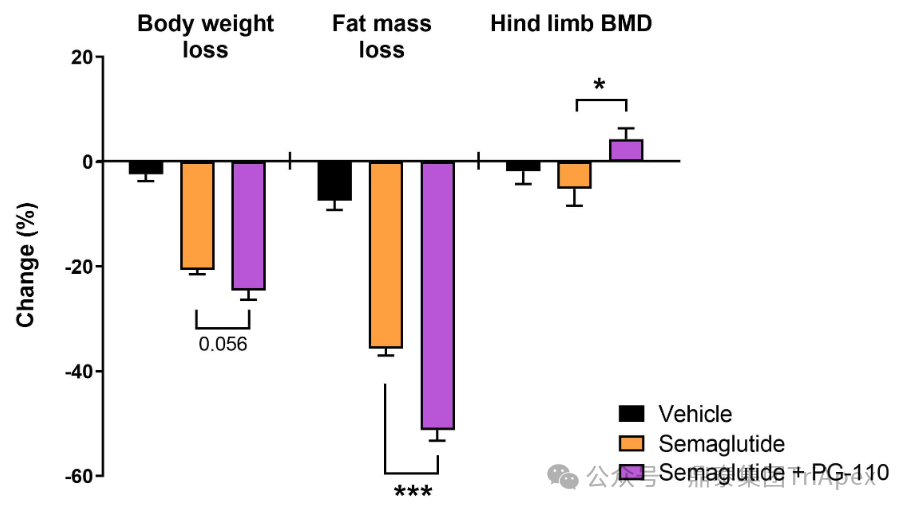
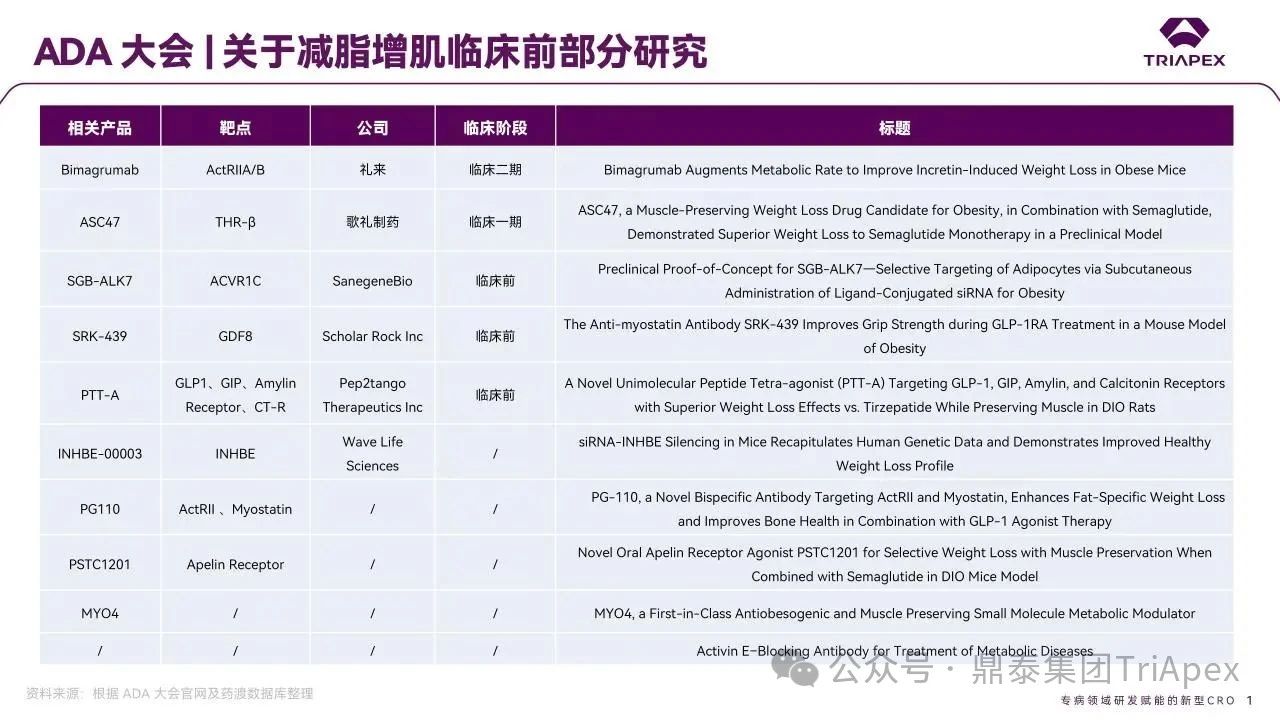
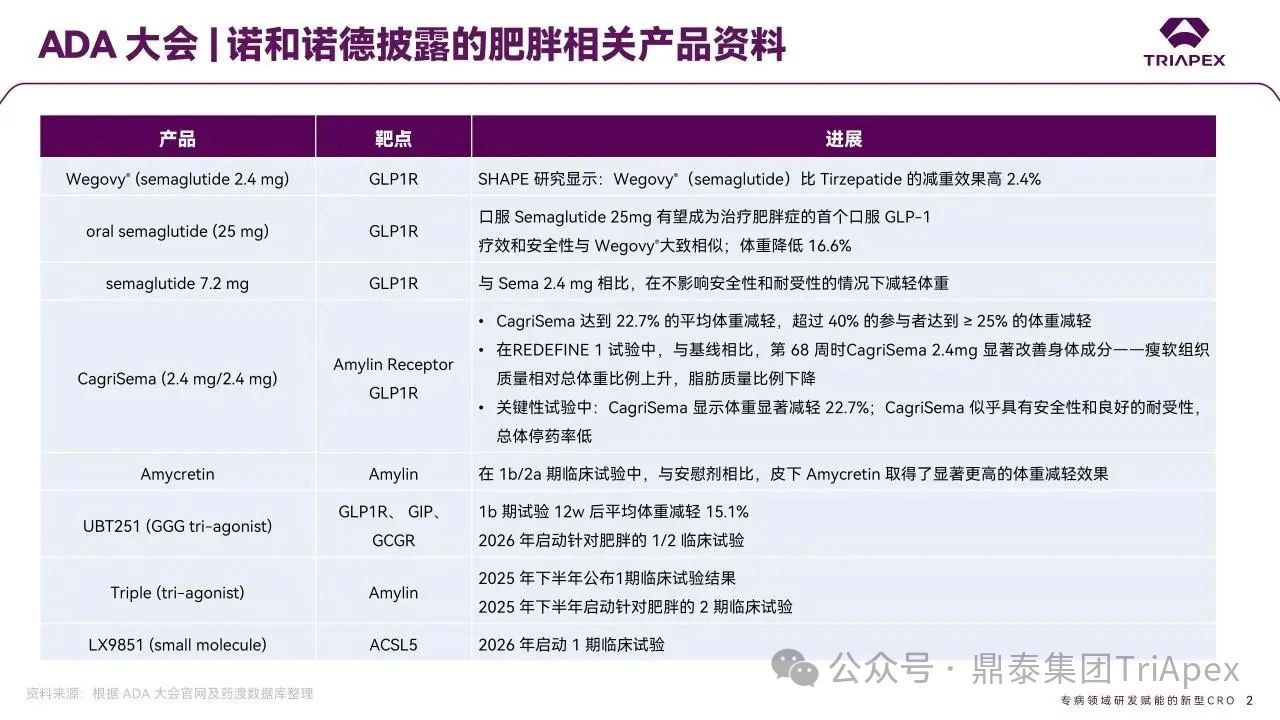
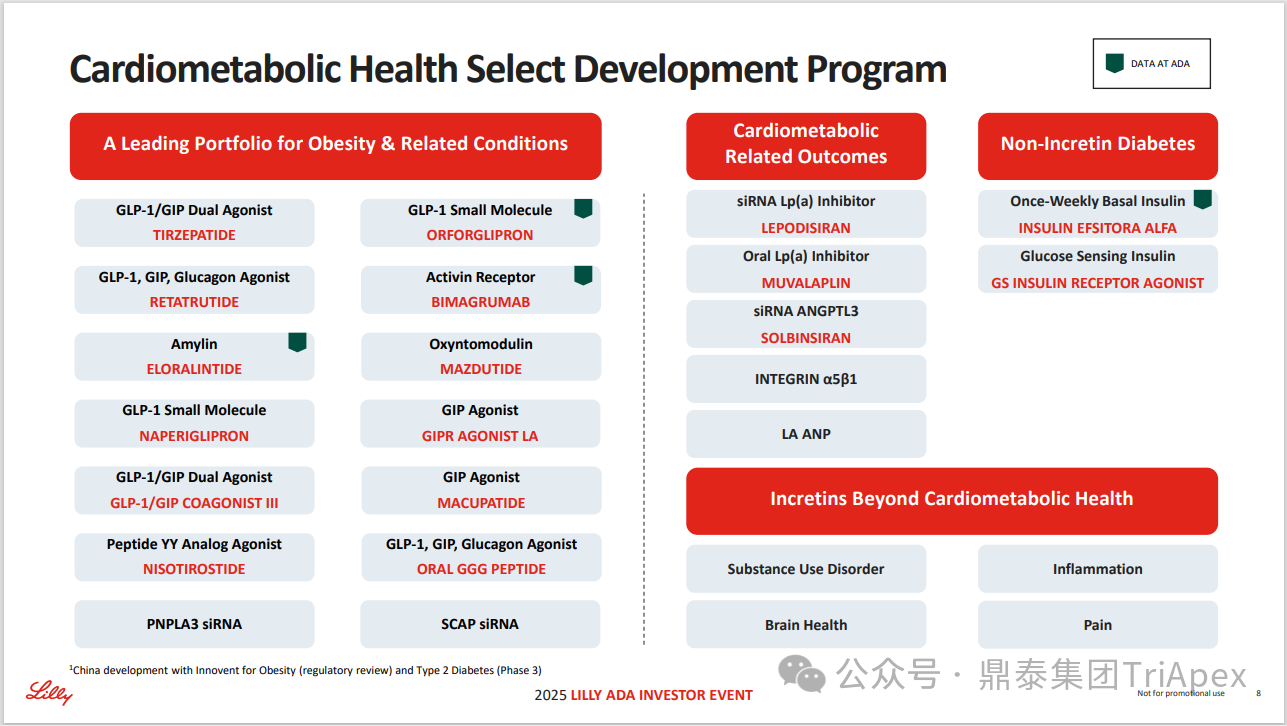
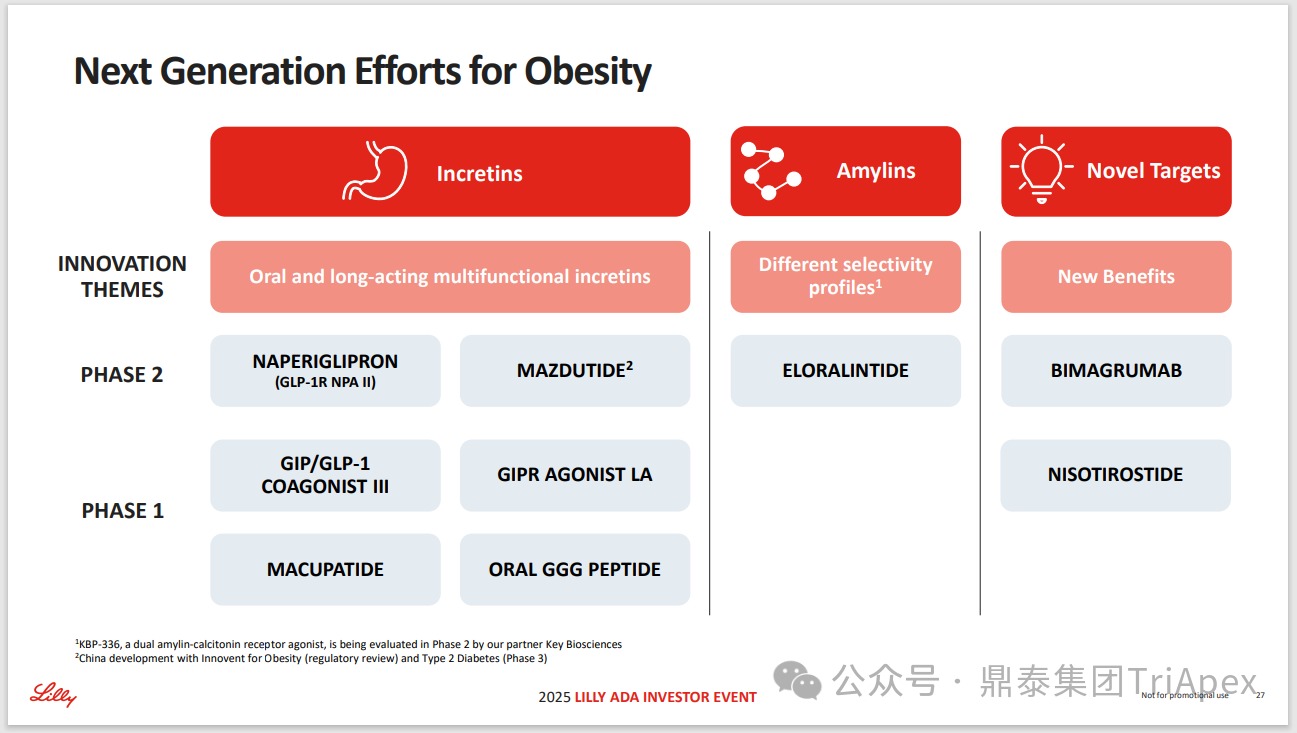
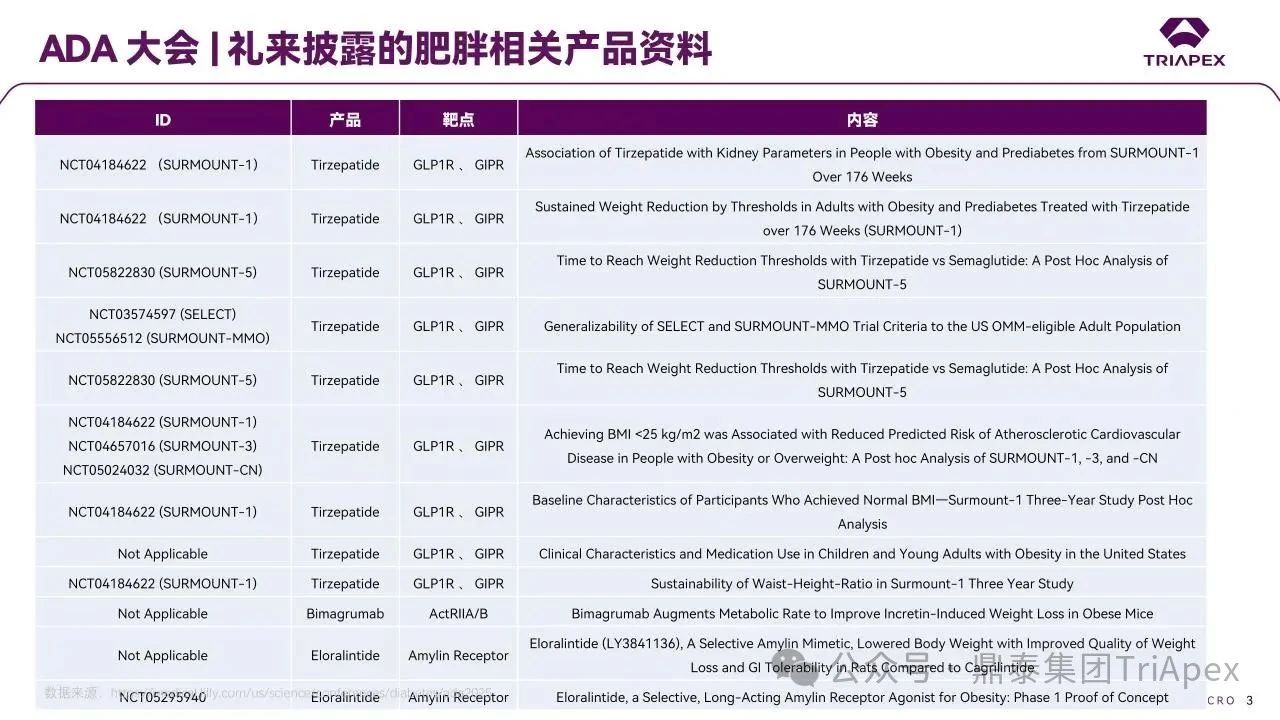
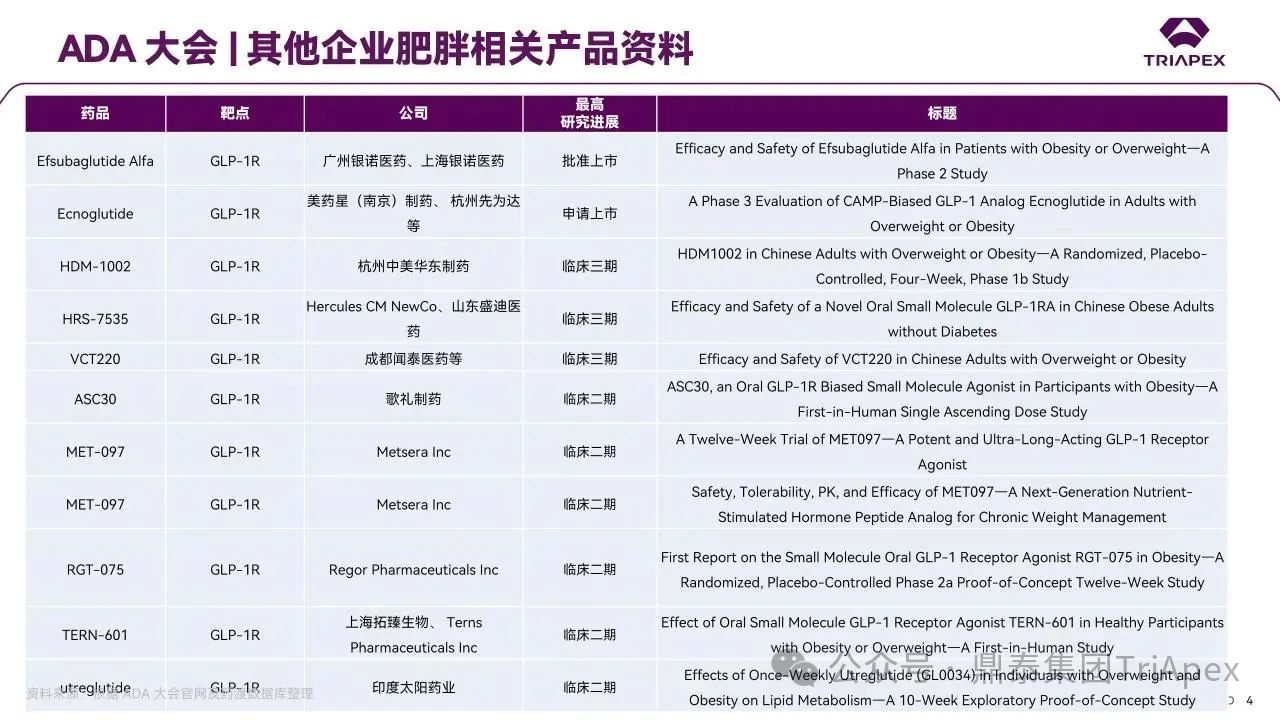
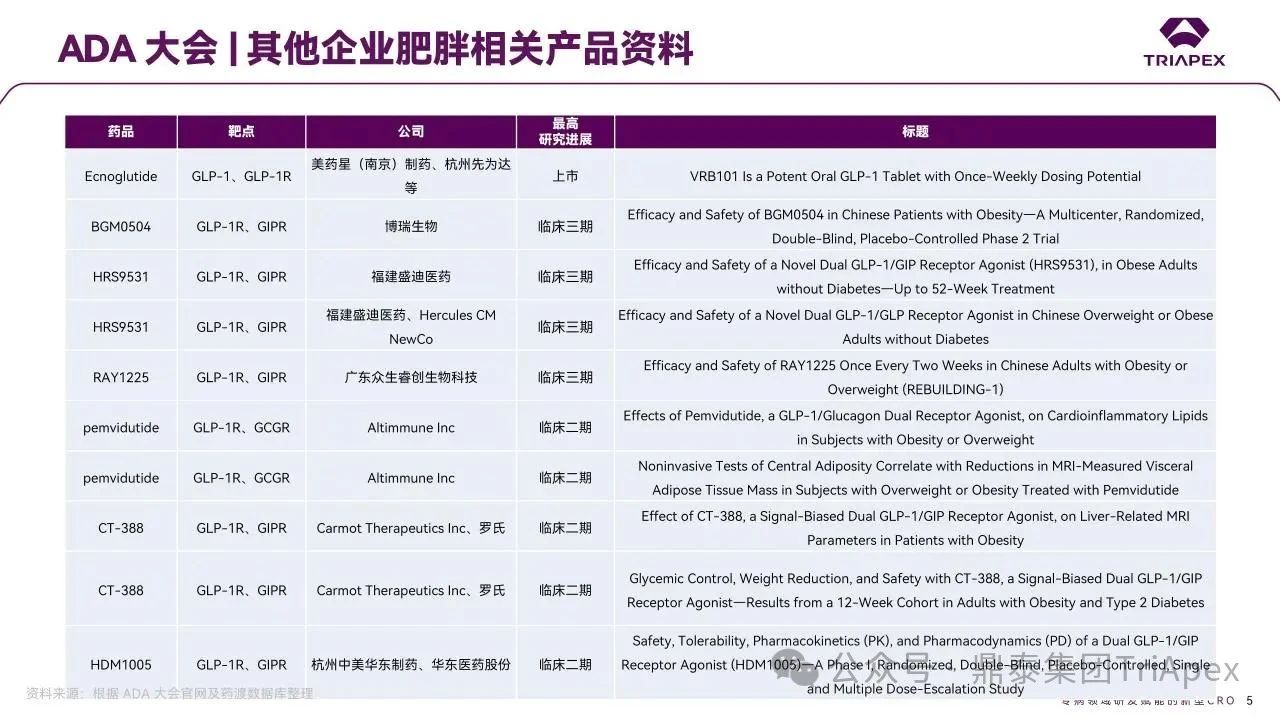
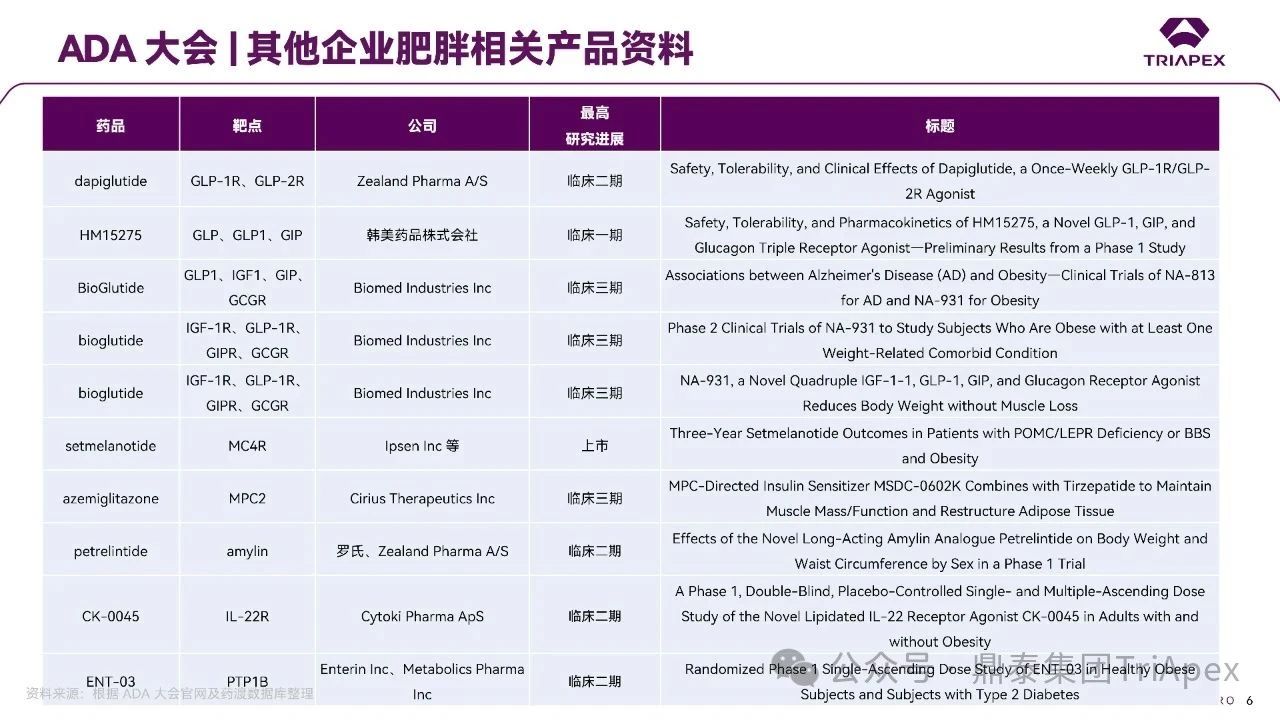
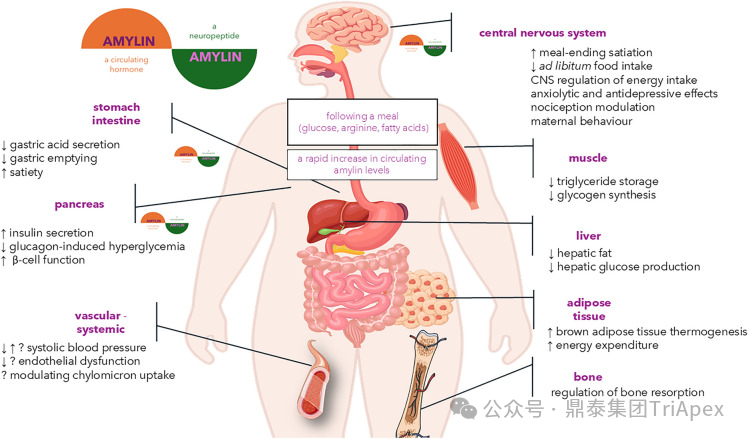
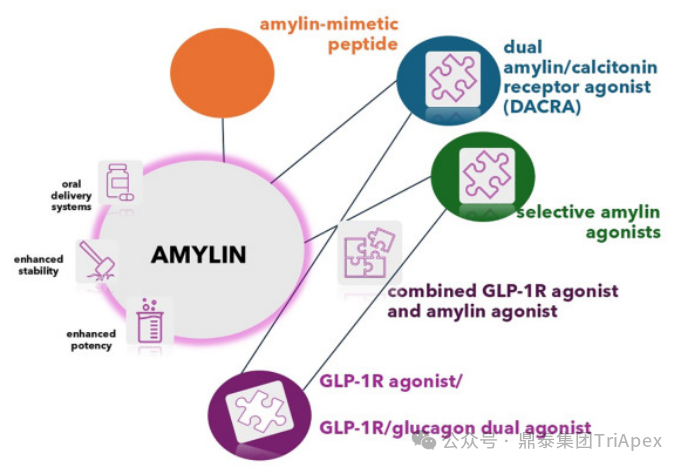
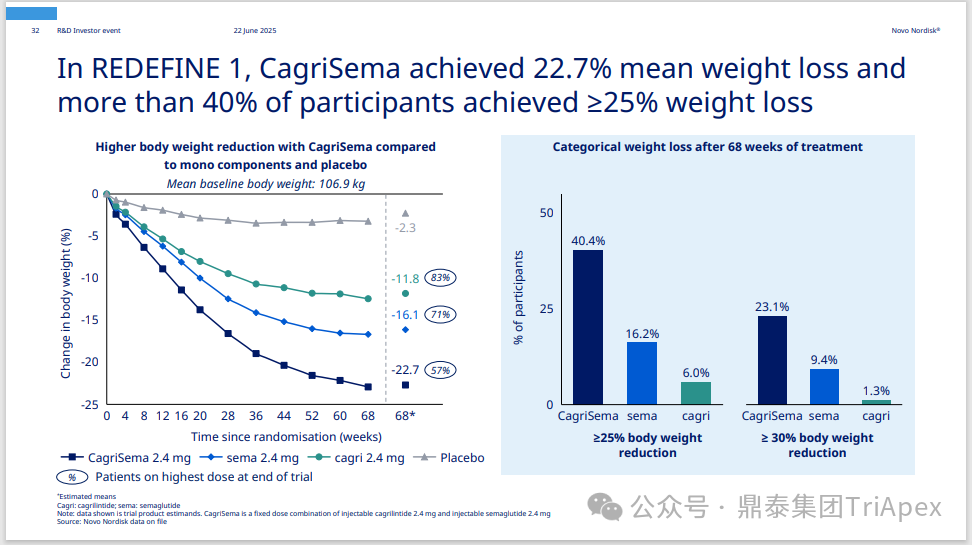
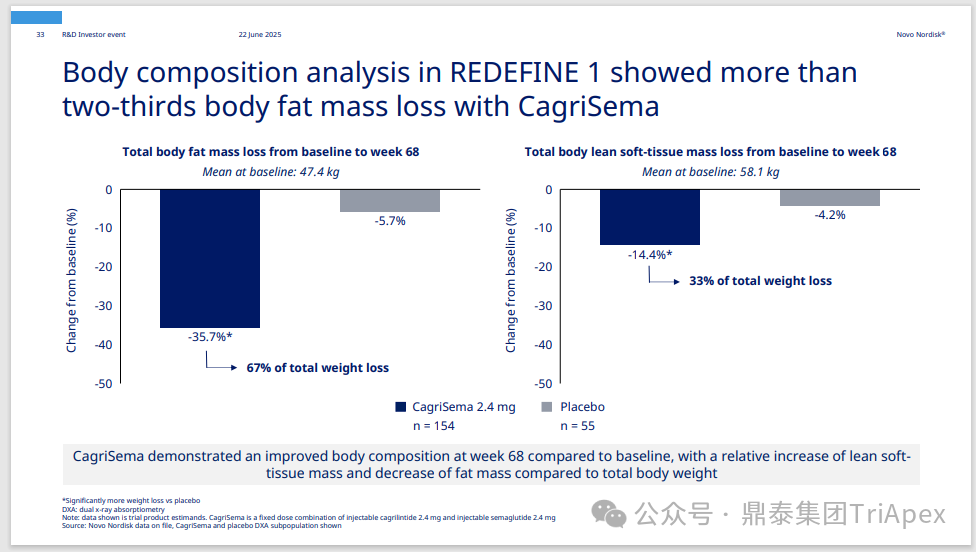
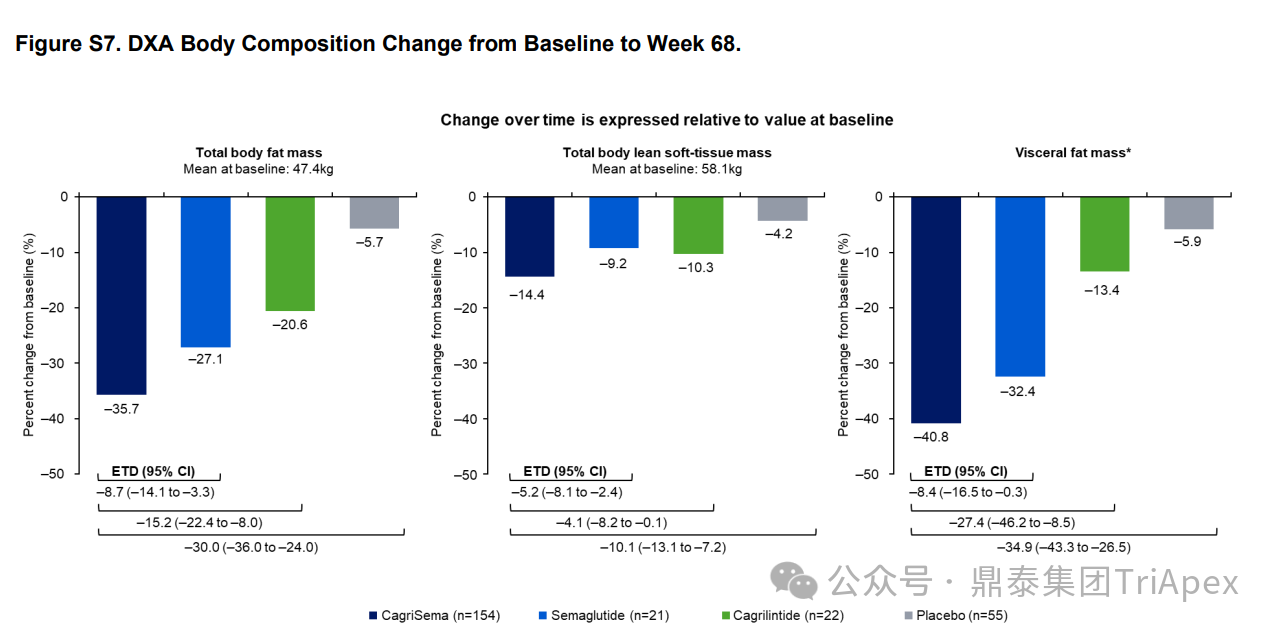
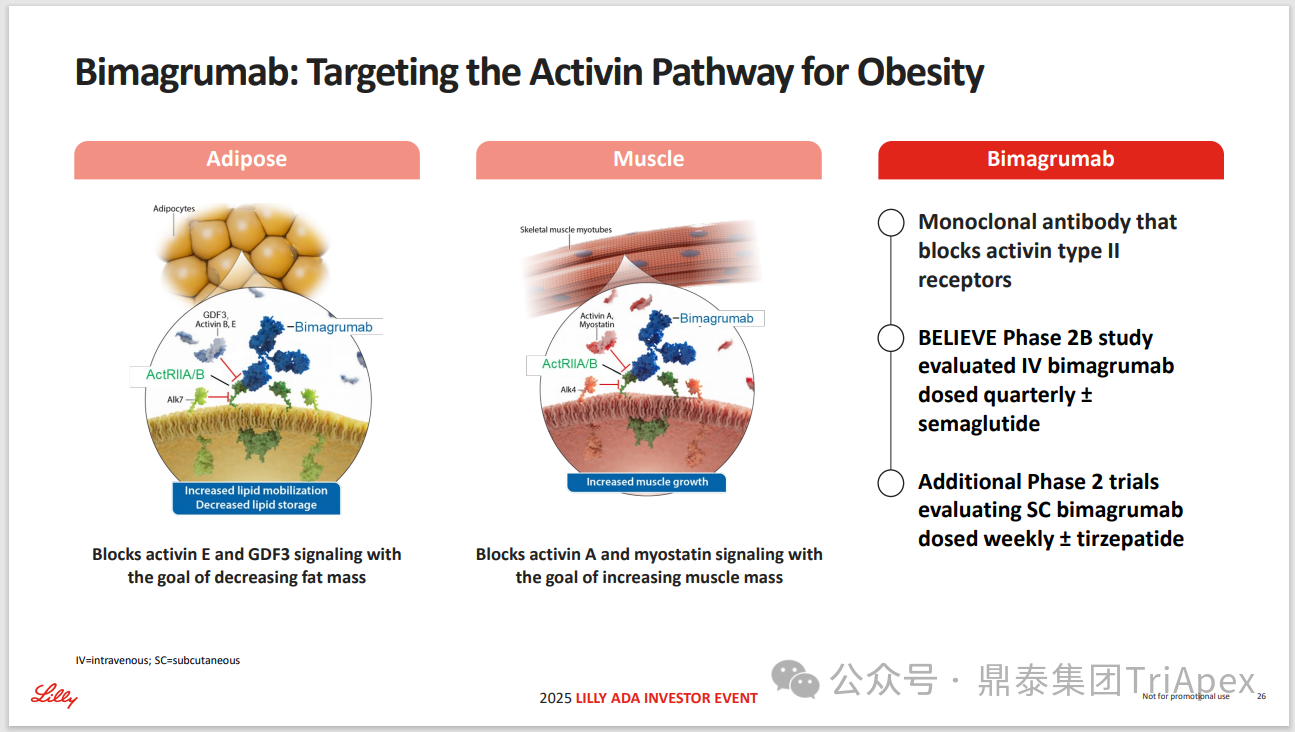
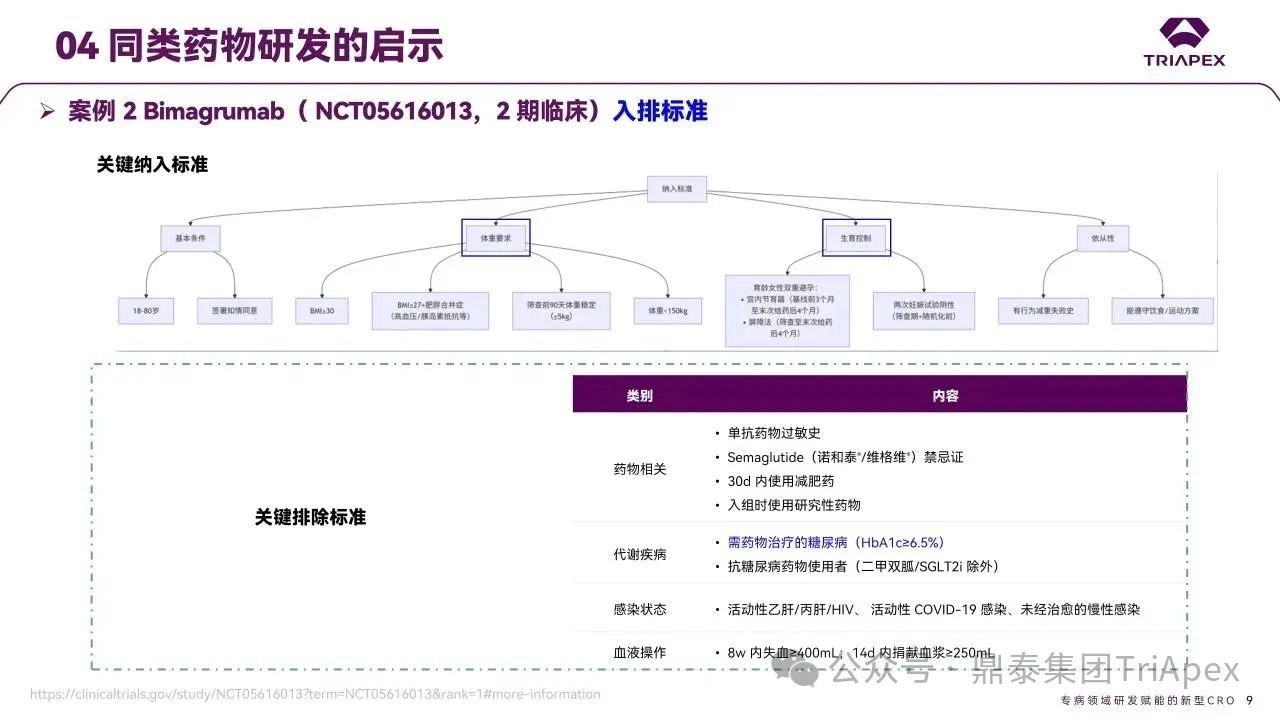
2025 年第 85 届美国糖尿病协会(American Diabetes Association,ADA)年度科学会议于 2025 年 6 月 23 日在芝加哥圆满闭幕。作为全球糖尿病领域规模最大、影响力最深的学术盛会之一,ADA 年会不仅是糖尿病预防、治疗与管理最新突破的展示平台,更是行业未来发展趋势的重要风向标。本次会议上汇聚了全球顶尖的科研机构、临床专家及创新企业,共同聚焦糖尿病预防、治疗与管理的最新突破与未来趋势。此外,在本次大会上对备受瞩目的《2025年美国糖尿病诊疗标准》(Standards of Care in Diabetes — 2025)进行了更新,为相关领域提供了最新指导。 作为一家专注于代谢领域创新赋能的新型 CRO 企业,鼎泰集团(TriApex)始终关注着全球糖尿病与肥胖治疗领域的最新动态。旗下子公司昆明科灵(KBI)作为长期致力于该领域非人灵长类药理药效研究的机构,在本次 ADA 年会上展示了其在糖尿病与肥胖治疗方面的重磅研究成果,进一步彰显了其在代谢疾病研究中的探索与洞察。 本文将重点回顾 2025 ADA 年会中围绕健康体重管理领域展现的最新研究进展、创新管线组合以及代表性药物研究进展等内容,以期为未来健康体重管理药物的研发和临床实践提供有价值的参考与启发。同时,我们也希望通过此次总结,进一步推动行业对代谢性疾病防控的关注与投入。 ★ 文章导览 ★ 01 健康体重管理的新方向 02 “减脂增肌”研发策略下的多样化管线 2.1 临床前管线研究进展 2.2 临床管线研究进展 03 健康减重产品代表性研究进展 3.1 CagriSeama 3.2 Bimagrumab 04 科灵生物携重磅研究成果亮相 ADA 2025 健康体重管理的新方向 GLP-1 受体激动剂(GLP-1RA)凭借显著的降糖、减重效果和代谢获益,已成为全球糖尿病和肥胖症药物治疗的基石。在众多在研靶点中,GLP-1R 依然是糖尿病和肥胖症治疗领域的核心,并在此基础上衍生出更多的新靶点或新疗法的组合创新。截至目前,全球已有数十款产品上市,数百款产品处于临床开发阶段。在众多的新药开发企业中,礼来和诺和诺德稳居全球领先地位,同时,研发热潮也助推了很多新的潜力公司的出现(详见 02 “减脂增肌”研发策略下的多样化管线)。 图1. 在研 GLP-1RA 研发现状 当前,全球研发企业正加速拓展多元化产品管线的布局: 成熟靶点的组合创新:从单靶点向多靶点协同演化,如 GLP1R → GLP1R/GIPR;GLP1R/GCGR;GLP1/GIPR/GCGR 等。 新作用机制的互补与协同:探索多作用机制靶点的组合,如 Amylin/ GLP1R。 潜力靶点挖掘与 New Modality 涌现:积极开发新兴潜力靶点,如 ActRIIA/B、INHBE、ALK7、GDF8、THR-β、ACSL5 等;分子类型也不在局限于化学合成多肽,而是进一步扩展到单抗/双抗、融合蛋白、寡核酸药物和化学小分子等。其中,关于 INHBE、ALK7 等靶点,往期推文已进行了深度剖析: 越来越多的研究显示,GLP-1RA 在显著减轻体重的同时伴随瘦体重减少,并成为其临床应用的痛点。研究表明,GLP-1RA 治疗期间,瘦体重(肌肉)流失占总体重减轻的比例高达 20%-50%。 图2. “饮食干预、GLP-1R 或 GLP-1R/GIPR 激动剂治疗、减肥手术”导致的瘦体重减少和体重减少之间的关系 表1. 临床试验中 GLP-1RA 产品对瘦体重的影响 随着人们对 GLP-1RA 治疗过程中体重流失等问题的认识加强,体重管理药物的研发方向也在不断优化,重点聚焦于: 延长给药间隔,以提高便利性和依从性 提高安全性,延长用药时长 拓展新的适应症,挖掘更多的临床获益 在这种趋势下,该领域的临床开发目标不再仅仅在于高效减脂,更需关注肌肉质量的维持以及长期疗效的巩固。因此,“减脂增肌”成为当下产品迭代的核心趋势,各公司正竞相投入“增肌”产品的研发,其中以礼来和再生元最为积极,也不乏来凯生物、Rock Scholar 等新兴生物技术公司。 下文将聚焦本次会议上关于肥胖症治疗的最新研发进展,重点聚焦于“减脂增肌”产品的代表性管线,深入剖析其科学价值与临床应用前景,并探讨相关潜力靶点的研究现状与未来发展趋势。 “减脂增肌”研发策略下的多样化管线 本部分内容根据 2025 年 ADA 科学年会公开的信息进行梳理,重点关注糖尿病和肥胖症治疗领域的新机制靶点、代表产品及临床进展。 1 临床前管线研究进展 当前减脂增肌产品的临床前研究聚焦于解决 GLP-1RA 类药物(如 Semaglutide、Tirzepatide)的核心痛点 —— 减重过程中的瘦体重流失问题,通过联合疗法或新靶点产品实现健康减重。 本次大会公布的临床前数据关联的部分产品如下: Bimagrumab(抗 ACVR2A/B 抗体,Lilly) ASC47(选择性 THR-β 激动剂,歌礼制药) SGB-ALK7(靶向脂肪细胞 ALK7 siRNA,SanegeneBio) SRK-439(抗 Pro/Latent Myostatin 抗体,Scholar Rock) PTT-A(GLP-1、GIP、Amylin 和 Calcitonin 受体激动剂,Pep2tango) PSTC1201(Apelin 受体激动剂) PG-110(靶向 ActRII 和 Myostatin 的新型双特异性抗体,ProGen) INHBE siRNA(GalNac siRNA,Wave Life Sciences) Ø Bimagrumab —— 特异性地结合到激活素 Ⅱ 型受体,阻止天然配体(如 Activin、GDF 11 等)与其结合,改善肠促胰岛素(Incretin)诱导的肥胖小鼠肥胖 TGF-β 家族配体通过和骨骼肌和脂肪组织中的激活素 Ⅱ 型受体(ActRII)结合激活下游信号通路,对肌肉生长产生负面影响并促进过度肥胖。 在动物试验中,Bimagrumab 治疗增强了 GLP-1RA 和 Tirzepatide(双靶点激动剂)诱导的体重减轻。Bimagrumab 与 Incretin 类药物联用时,可通过增强脂肪质量减少并抑制瘦体重流失,提供了更健康的减重效果。 Ø ASC47 —— 一种肌肉保护型肥胖治疗药物, 在临床前模型中与 Semaglutide 联用的减重效果优于 Semaglutide 单药治疗 ASC47(小分子 THR-β 激动剂)与 Semaglutide 联用可以通过保护肌肉达到健康减重。C57BL/6J 小鼠高脂饲养 16W,接受不同处理 28d。每天记录体重和食物摄入量,每周通过 EchoMRI 评估身体成分。治疗结束时,接受 ASC47 低剂量联合治疗的肥胖小鼠总肌肉质量占总体重百分比达 68.8%,接近健康非肥胖小鼠水平(66.0%),表明该方案实现了健康减重。 表2. ASC47 低剂量联合治疗在减重方面优于 Semaglutide 单药治疗 Ø SGB-ALK7 —— 通过配体偶联 siRNA 皮下给药选择性靶向脂肪细胞 SanegeneBio 正在开发配体-增强剂辅助递送(LEAD™)技术。 该技术利用受体介导的内化机制,实现靶向脂肪细胞生物分布、降低肝脏靶向性(de-target liver)的双重目标。SGB-ALK7 基于此平台开发,其是一种有效的 siRNA 治疗药物,可敲减脂肪中 ALK7,在保持瘦体重的同时减少脂肪量,并促进体重减轻。 在非人灵长类动物中证实,单次皮下给药后可实现持久且组织选择性的脂肪细胞目标 mRNA 抑制。在 DIO 小鼠模型中,SGB-ALK7 体重减轻效果与 Semaglutide 相当,同时实现接近完全的瘦体重保留。 图3. SGB-ALK7 在体重减轻方面与 Semaglutide 相当;SGB-ALK7 减少 Semaglutide 停用引起的体重增加;SGB-ALK7 增强并提高 Semaglutide 的减肥效果 Ø SRK-439 —— 改善了 GLP-1RA 治疗在小鼠肥胖模型中的握力 DIO 小鼠同时用 SRK-439(anti-pro/latent myostatin antibody)或 IgG 对照联合Semaglutide 治疗 5W。SRK-439 可抵消 Semaglutide 的肌肉副作用,实现瘦体重净增长。 Ø PTT-A(新型靶向 GLP-1、 GIP、Amylin 和 Calcitonin Receptors 的四靶点激动剂) —— 在 DIO 大鼠中,与 Tirzepatide 相比具有优异的疗效,同时保留肌肉 对 DIO 大鼠给予 PTT-A (30nmol/kg) 治疗 3W, 19.2% 体重降幅完全源于脂肪减少。 Ø PG-110 —— 一种靶向 ActRII 和 Myostatin 的双特异性抗体,与 GLP-1RA 联用,可增强脂肪特异性体重减轻并改善骨骼健康 用 Semaglutide(QD)和 PG-110(QW) 处理饮食诱导的 C57BL6/N 肥胖小鼠 2W,检测体重和身体成分以评估对脂肪量、肌肉量和骨矿物质密度的影响。结果显示,Semaglutide 单药有效降低体重;当与 PG-110 联合使用时,脂肪量减轻显著增强,整体体重减轻速度加快,未观察到瘦体重发生显著变化。此外,PG-110 治疗显著增加了后肢骨密度。 Semaglutide 与 PG-110 联合使用可增强脂肪特异性减重,并改善 DIO 小鼠骨密度,且不损害瘦体重。这些发现表明,当与基于肠促胰岛素的疗法( incretin-based therapies)结合使用时,PG-110 对于优化减脂和骨骼健康可能提供一种有前途的治疗策略。 图4. Semaglutide 与 PG-110 联用瘦体重变化 Ø INHBE siRNA —— 再现了人类遗传数据,并证明了改善的健康减肥概况 关于 INHBE 这个靶点以及相关 INHBE siRNA 的研究进展,本公众号在往期内容中已经有多次报道(点击查看原文)。 在 DIO 小鼠模型中, INHBE-00003(GalNAc-siRNA )单次给药后观察 28d。与 PBS 对照组相比,试验组体重降低 9%;饮食诱导的内脏脂肪积累减少 40%;股四头肌质量完全保留。Semaglutide 单药组:治疗 28d 后停药,至第 56d 时体重完全反弹;INHBE-00003 联用组:在第 21d 和 28d 追加 INHBE-00003,成功维持减重效果。 Ø 新型口服 Apelin 受体(APJ)激动剂 —— 与 Semaglutide 联合用于 DIO 小鼠模型的选择性减重(Selective Weight Loss)和肌肉保留 Apelin 是一种能与 APJ 结合的内源性肽,可调节能量和肌肉代谢。与 GLP-1RA 单药治疗相比,口服 APJ 激动剂联合 GLP-1R 可进一步减轻体重,同时改善体重组成和肌肉功能。DIO 小鼠用 Semaglutide(10 nmol/kg,Q3D)治疗 21d;相同剂量的 Semaglutide 与 PSTC1201(饮用水中 1.1 g/L)或 Azelapray 联用。测量体重、身体成分(通过 EchoMRI) 和肌肉功能(钢丝悬挂)、血糖和血脂水平。 Semaglutide 组、Semaglutide + Azelaprag 组、Semaglutide+PSTC1201 组小鼠体重分别减轻 11%、31% 和 37%,联用组瘦体重变化分别为 57% 和 57%,表明身体成分有所改善;在钢丝悬挂试验中,PSTC1201 治疗几乎使肌肉功能恢复到对照组(lean controls)的水平;空腹血糖和血脂也得到改善。PSTC1201 初步显示了进一步开发肥胖和糖尿病联合治疗的有利前景。 图5. ADA 大会 | 关于减脂增肌临床前部分管线研究进展 2 临床管线研究进展 ☆ 诺和诺德 诺和诺德凭借 GLP-1RA 领跑全球糖尿病治疗市场,通过 Semaglutide 在糖尿病和肥胖症领域建立了领导地位,并通过 CagriSema、Amycretin 及新型分子管线布局新一代疗法。 图6. 诺和诺德正在推进肥胖症的多样化治疗管线 图7. ADA 大会 | 诺和诺德肥胖相关管线进展 ☆ 礼来 礼来以 Tirzepatide 为基础,开发了下一代满足多样化需求的药物,通过靶点创新(多靶点/新机制)、新分子类型(多肽、siRNA、小分子化药)、给药技术(口服/长效注射)、适应症拓展(并发症管理)等进行了多维度产品布局,预计 2025 年至 2027 年将迎来多项关键临床数据或提交上市申请。 图8. 礼来心血管代谢健康选择开发计划 图9. 礼来肥胖症治疗计划 图10. 礼来肥胖症治疗策略 图11. ADA 大会 | 礼来肥胖相关管线进展 ☆ 其他 在本次 ADA 大会上,众多国内企业开始在该领域崭露头角。恒瑞医药、博瑞医药、杭州先为达、来凯医药、华东制药等十余家中国企业参加本次大会,并凭借差异化管线,跻身全球糖尿病、肥胖治疗的竞争核心圈,未来 2-3 年预计有多款产品实现临床突破。 图12. ADA 大会 | 其他企业肥胖相关管线(1) 图13. ADA 大会 | 其他企业肥胖相关管线(2) 图14. ADA 大会 | 其他企业肥胖相关管线(3) 健康减重产品代表性研究进展 1 CagriSeama Amylin 是一种与胰岛素共同分泌的神经内分泌激素,在葡萄糖调节中发挥作用,除了对食欲和体重控制有明确的影响外,还具有潜在的心血管和神经保护功能。由于 GLP-1 RA 和 Amylin 类似物诱导的体重减轻具有不同且重叠的机制,GLP-1 RA 和 Amylin RA 的组合已被证明可产生协同效应。下文以本次 ADA 大会公布的 CagriSeama 数据,解析双靶点联合的临床进展。 图15. Amylin 的器官特异性生理作用 图16. Amylin 靶点药物相关药物的类别 CagriSeama 是靶向 GLP1RR 和 Amylin 受体的双重激动剂。2025 年 6 月 22 日,诺和诺德公布了 CagriSema 首个关键临床 Ⅲ 期试验 REDEFINE 1(旨在探索 CagriSema 在超重或肥胖人群中的应用)相关数据: CagriSema 可达到 22.7% 的平均体重减轻,超过 40% 的参与者体重减轻 ≥25% 与基线相比,第 68w 时 CagriSema 2.4mg 显著改善身体成分 —— 瘦软组织质量(Lean soft-tissue body mass)相对总体重比例上升,脂肪质量比例下降 CagriSema 具有安全性和良好的耐受性,总体停药率低 Ø 试验设计 参与者:3,417 例超重/肥胖患者(BMI ≥30 或 ≥27 合并肥胖相关并发症),排除糖尿病患者 方案:随机分配至 CagriSema 2.4mg、Semaglutide 2.4mg、Cagrilintide 2.4mg 或安慰剂组 主要终点:68w 体重相对基线变化率、≥5% 体重减轻比例 图17. REDEFINE 1 临床试验设计 Ø 试验结果 - 减重效果、身体成分分析 CagriSema 治疗组通过体重秤测量,平均体重减轻为 26.6kg,而安慰剂组为 3.6kg。在一项预设分析中,3417 名参与者中有 252 人(7.4%)接受了 DXA 扫描以评估身体成分。该亚组基线时平均总脂肪质量为 47.4kg,平均瘦体重为 58.1kg。通过 DXA 评估,CagriSema 组从基线至第 68w 的总脂肪质量和瘦软组织质量的绝对减少量分别为 -17.0kg 和 -8.4kg(相当于总减重量的 67% 来自脂肪减少,33% 来自瘦软组织减少),而安慰剂组分别为 -3.4kg 和 -2.6kg。CagriSema 组基线时总脂肪质量平均占比为 44.0%,瘦软组织质量平均占比为 53.5%。该组总脂肪质量和瘦软组织质量从基线至第68w的百分比变化分别为 -35.7% 和 -14.4%,而安慰剂组分别为 -5.7% 和 -4.2%。 接受 CagriSema 治疗的参与者观察到有利的身体成分变化:具体表现为脂肪质量减少比例(67%)高于瘦软组织质量减少比例(33%)。 图18. Cagrisema 实现了 22.7% 的平均体重减轻,并且超过 40% 的参与者实现了 ≥25% 的体重减轻 图19. Cagrisma 可引起超过 2/3 脂肪质量丢失 图20. DXA 身体成分从基线到第 68w 的变化 2 Bimagrumab 在本次 ADA 大会上,礼来在专题研讨会上公布了 Bimagrumab 和 Semaglutide 联合使用的研究结果。 Bimagrumab 是一种首创的靶向激活素 Ⅱ 型受体,能促进肌肉保存和增长,作用机制: 脂肪组织:阻新 Activin E 和 GDF3 信号传导,减少脂肪质量(脂质动员增加,脂质储存减少) 肌肉组织:阻断 Activin A 和 Myostatin 信号传导,以增加肌肉质量(增加如肌肉生长) BELIEVE 2b 期试验是一项随机、双盲、安慰剂对照、多中心研究,旨在评估 Bimagrumab 联合 Semaglutide 治疗能否在体重和/或脂肪量下降的同时维持或增加肌肉量。 图21. Bimagrumab 作用机制 507 名参与者接受了每周一次的 Semaglutide 皮下注射和/或在第 4、16、28 和 40w 通过静脉输注给予的 Bimagrumab。主要终点是体重相对于基线的变化。次要终点包括腰围、全身脂肪量、内脏脂肪组织和瘦体重的变化等。 图22. Bimagrumab NCT05616013 临床试验设计 图23. Bimagrumab NCT05616013 试验终点 图24. Bimagrumab NCT05616013 入排标准 结果表明,与任一单药治疗相比,Bimagrumab 与 Semaglutide 联合疗法在减轻体重、体脂、内脏脂肪以及炎症标志物方面效果更显著。联合疗法带来的体重减轻中,有 92.8% 来自脂肪减少,而单用 Semaglutide 为 71.8%;联合疗法使体重下降了 22.1%(单用 Bimagrumab 组为 −10.8%;单用 Semaglutide 组为 −15.7%)。值得关注的是,单用 Bimagrumab 时,体重减轻完全(100%)归因于脂肪减少,且总瘦体重增加了 2.5%。此外,研究人员正在研究 Bimagrumb 与 Tirzepatide 联合使用,以评估其对疗效和安全性的双重影响。 除此之外,在减脂增肌领域还有很多值得期待的新机制、新组合、新分子类型或新的临床试验设计的研究进展,鼎泰团队会持续对该领域的最新进展进行持续关注。 科灵生物携重磅研究成果亮相 ADA 2025 GLP-1RA 尽管在降糖和体重管理方面取得了突破性的进展,同时瘦体重流失的风险也正在驱动企业探索新型研发策略,如开发 TGF-β 信号通路相关靶点的抗体、融合蛋白或 siRNA 产品(如激活素受体、ALK7、INHBE),或是与 GLP-1RA 联用,或开发多靶点产品等方式,推动减重疗法向体成分优化方向迭代。在从实验室研究向临床转化的过程中,鼎泰集团始终站在行业需求的最前沿。截至目前,已开展了多项该领域 siRNA、单抗、多肽和融合蛋白类药物的非临床研究。 在本届 ADA 大会上,科灵生物精心布置了展位(Booth#3131),并借助成果壁报(编号:1707-P)展示了最新研究成果,该研究聚焦于使用钡餐法直接评估司美格鲁肽治疗对非人灵长类动物胃排空动力学的影响,并将其与间接的对乙酰氨基酚吸收动力学方法进行了比较。 供稿:转化科学和药政策略部 声明:本文系药方舟转载内容,版权归原作者所有,转载目的在于传递更多信息,并不代表本平台观点。如涉及作品内容、版权和其它问题,请与本网站留言联系,我们将在第一时间删除内容