
2026-01-07 09:17:46来源:医药魔方浏览量:934
2025年,国家药品监督管理局(NMPA)共批准127款新药,包括81款化药(含小分子、多肽及核酸等)、40款生物药(含单抗、双抗、ADC、细胞疗法等)、6款中药。与往年相比,2025年NMPA批准新药数量显著上涨,为近六年来最高值。
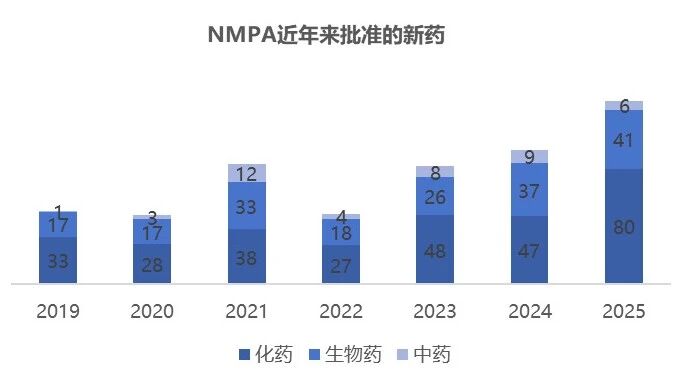
注:数据来源于医药魔方PharmaGo数据库。NMPA批准新药定义为在中国首次获批上市的新分子实体(以及包含有新分子实体的复方)、生物药、中药和疫苗,不包括生物类似物、新适应症、新剂型。
l 药物类型
从药物类型来看,小分子药物依旧是2025年NMPA批准新药上市的主流,占比高达57%(72款)。紧随其后的品类中,单抗药物有18款获批;多肽与双抗药物分别有4款获批;ADC、融合蛋白及细胞疗法均有3款获批。
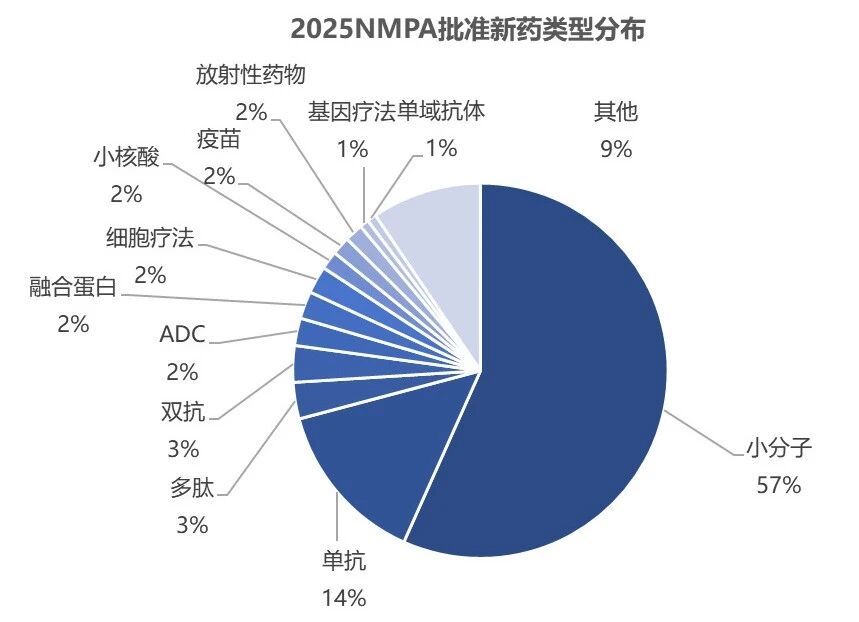
l 疾病领域
肿瘤领域依然是2025年中国创新药获批上市的热门,其中又以乳腺癌最为火热,全年共有9款新药获批,包括PI3Kα抑制剂伊那利塞、AKT抑制剂卡匹色替,以及多款CDK抑制剂(吡洛西利、来罗西利、泰瑞西利、伏维西利、库莫西利),此外还有TROP2 ADC德达博妥单抗、HER2 ADC博度曲妥珠单抗等。
乳腺癌之外,非小细胞肺癌、前列腺癌、卵巢癌等实体瘤领域也迎来多款突破性疗法。例如,靶向EGFR/c-Met的埃万妥单抗、KRAS G12C抑制剂戈来雷塞、靶向VEGF-A的苏维西塔单抗,以及放射性药物镥[177Lu]特昔维匹肽、镓[68Ga]戈泽肽等,进一步丰富了实体瘤的靶向治疗手段。
血液肿瘤领域同样不乏亮点,多款创新产品成功获批,包括EZH2抑制剂泽美妥司他、Bcl-2抑制剂索托克拉与利沙托克拉等,为血液系统恶性肿瘤患者提供了新的治疗选择。
肿瘤领域之外,心血管和代谢疾病是2025年新药获批的另一重要阵地。其中,2型糖尿病领域共有6款新药上市,涵盖复方制剂(恒格列净瑞格列汀二甲双胍、二甲双胍瑞格列汀)、DPP-4抑制剂普卢格列汀、CD3替利珠单抗,以及GLP-1R激动剂依苏帕格鲁肽α。值得关注的是,玛仕度肽不仅获批2型糖尿病适应症,同时拿下减重适应症,成为代谢领域的重磅产品。
此外,罕见病与免疫疾病领域获批上市的创新药产品持续增加。全年共有波哌达可基、芬妥司兰、维拉苷酶β等多款罕见病治疗药物获批,为罕见病患者带来“救命药”。免疫疾病领域则迎来利生奇珠单抗、罗泽利昔珠单抗、瑞米布替尼等新药,进一步满足自身免疫性疾病患者的临床需求。
l 国产创新药
2025年,国产创新药延续强劲发展势头,在NMPA批准的127款新药中,国产新药占比达55%,共计70款。这些国产新药覆盖小分子、抗体类、细胞疗法、中药等多种药物类型,治疗领域遍布肿瘤、代谢、免疫、罕见病等多个关键赛道。
国产创新药的崛起不仅体现在数量上,更在创新水平层面实现多项突破。2025年,信达生物的玛仕度肽成功上市,成为全球首款获批的GLP-1R/GCGR双靶点激动剂;万泰生物的九价人乳头瘤病毒疫苗(大肠埃希菌)获批,成为国内首个上市的9价HPV疫苗;亚盛医药的利沙托克拉获批上市,成为中国首个用于治疗慢性淋巴细胞白血病/小淋巴细胞淋巴瘤(CLL/SLL)的Bcl-2抑制剂。
企业层面,国产药企的创新产出能力持续凸显。恒瑞医药以9款新药获批的成绩位居国产药企首位,涵盖7款小分子药物、1款ADC药物及1款单抗;复星医药、信达生物、东阳光药、华东医药、诺诚健华等企业也均有多款药物获批,形成了多元化的创新药企梯队。
l 进口创新药
2025年NMPA共批准了57款进口药物,涉及的治疗领域广泛且创新药物类型丰富,其中不乏first-in-class药物,如全球首个靶向抗凝血酶的siRNA疗法芬妥司兰钠、全球首个靶向治疗免疫性血栓性血小板减少性紫癜(iTTP)的纳米抗体药物卡拉西珠单抗等。
公司层面,诺华以6款新药获批的成绩领跑跨国药企,涵盖3款小分子药物、2款放射性药物及1款单抗;赛诺菲、阿斯利康、强生等巨头也均有多款新药在中国上市,持续深化在华创新布局。
未来,随着审评审批体系的持续优化与本土创新能力的不断提升,有望迎来更多适配中国患者需求的优质新药。
附表:2025年NMPA批准的新药

声明:本文系药方舟转载内容,版权归原作者所有,转载目的在于传递更多信息,并不代表本平台观点。如涉及作品内容、版权和其它问题,请与本网站留言联系,我们将在第一时间删除内容