
2026-05-07 10:48:09来源:药方舟浏览量:8
本周(4 月 28 日 - 5 月 4 日)恰逢 "五一" 假期前夕,国内创新药 BD 领域延续 Q1 以来的火爆态势。据医药魔方数据,2026 年 Q1 中国创新药对外 BD 交易总额达 614 亿美元,占全球交易 69.7%,同比增长 66.4%,全年交易规模有望突破 1500 亿美元。
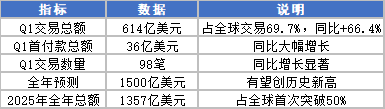
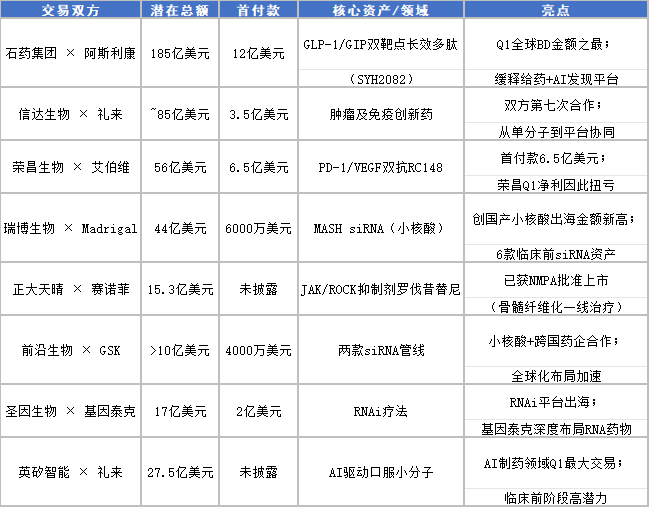
·小核酸:Q1合计71.6亿美元,已超过2025年全年,GLP-1、代谢疾病、MASH领域为核心驱动力
·双/多抗:VEGF/PD(L)1双抗占BD出海TOP10案例半壁江山,CD3+双抗持续受MNC青睐
·口服多肽:GLP-1赛道持续火热,石药/阿斯利康185亿美元合作树里程碑
·AI制药:技术平台合作成为MNC核心诉求,从单分子授权向"平台+能力"捆绑转变
ADC:Q1仅4笔对外授权,热门靶点EGFR、CLDN18.2、B7-H3、TROP2赛道竞争激烈,但"复购"信任基础已建立
【生物医学新技术临床转化管理条例】
2026年5月1日,国务院令第818号——《生物医学新技术临床研究和临床转化应用管理条例》正式落地实施。这是我国首部专门针对细胞治疗、基因编辑、基因治疗等前沿生物医学技术的行政法规,标志着我国对新兴治疗技术的监管进入规范化、法治化新阶段,对创新生物药的临床转化具有重要指导意义。
【最高法/最高检:医疗领域行贿严惩】
两高联合发布《关于办理贪污贿赂刑事案件适用法律若干问题的解释(二)》,明确医疗领域行贿10万元即可入刑,大幅降低医疗反腐追诉门槛,"带金销售"模式面临系统性刑事追责风险。
2025年12月31日国务院第76次常务会议修订通过《药品管理法实施条例》,自2026年5月15日起施行。该条例系23年来首次全面修订,修改条款超过90%,对创新药产业影响深远:
◆ 鼓励药品创新(核心主线):支持以临床价值为导向的药品研制;鼓励新药临床推广;正式确立突破性治疗药物、附条件批准、优先审评审批、特别审批四大快速通道的法律地位
◆ 市场独占期制度(首次立法):儿童用药品:获批后12个月市场独占期;罕见病药品:12个月(存在有效治疗手段)或24个月(无有效治疗手段);同步要求保障药品供应
◆ 临床试验申办者变更机制:明确临床试验申办者可依法变更,为BD交易的管线转让提供法规路径,降低研发管线流转制度障碍,促进资源优化配置
◆ 境外临床数据认可:境外取得的研究数据,符合NMPA规定的可支持国内药品注册,推动国际多中心临床试验(IMCT),实现"一份数据、多国申报"
◆ 分段委托生产制度:允许上市许可持有人委托符合条件企业分段生产创新药、临床急需药品及突发公卫事件急需药品;打破"全工序必须在同一场地完成"的传统模式
◆ 商业规模批次有条件上市:新药、罕见病药、短缺药品在通过GMP符合性检查后,商业批次也可提前上市销售,大幅缩短患者等待时间
◆ 数据保护制度扩展:从"新型化学成份药品"扩展至"符合条件的其他药品",为细胞治疗、生物制品等创新药提供数据保护灵活性
ASCO(美国临床肿瘤学会)年会将于5月29日-6月2日在美国芝加哥召开。目前摘要标题已正式发布,中国创新药军团表现亮眼:
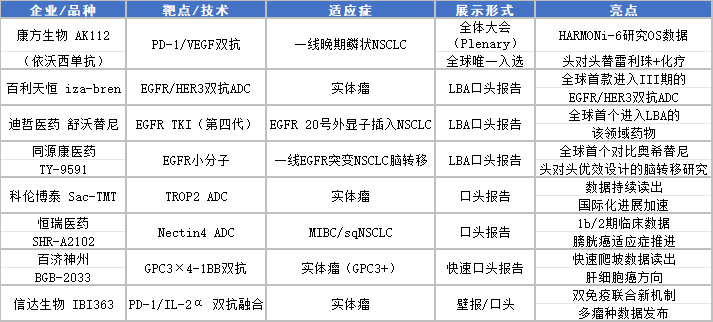
4月27日,药明康德一季报披露:单季收入124.4亿元,同比增长28.8%,归母净利润同比增长26.7%。小分子工艺研发和生产(DM)业务表现亮眼,CXO行业景气度回升信号明确,为创新药研发投入提供产能保障。
据医药魔方数据,2026创新药BD交易大会(BioPartnering 2026)即将于5月举办,届时1000+创新药BD负责人与投资人将汇聚,推动更多潜在合作落地。全年BD交易火热态势有望延续。
2026年以来的BD交易呈现显著结构性变化:早期项目(临床前至I期)占比66%,MNC不再仅购买"上市确定性",而是系统性地"购买未来可能性"和"技术平台能力"。石药/阿斯利康185亿美元合作即为典型——不仅授权8个多肽分子,更捆绑了多肽AI发现平台和缓释给药平台。这对国内创新药企业的平台化能力建设提出了更高要求。
【免责声明】本报告仅供行业参考,不构成投资建议。数据来源于医药魔方、医药出海通、新浪财经、NMPA官网等公开渠道,| 南京知和医药整理 统计口径存在差异,具体交易金额以企业公告为准。