
2026-04-08 15:52:33来源:转化医学网浏览量:198
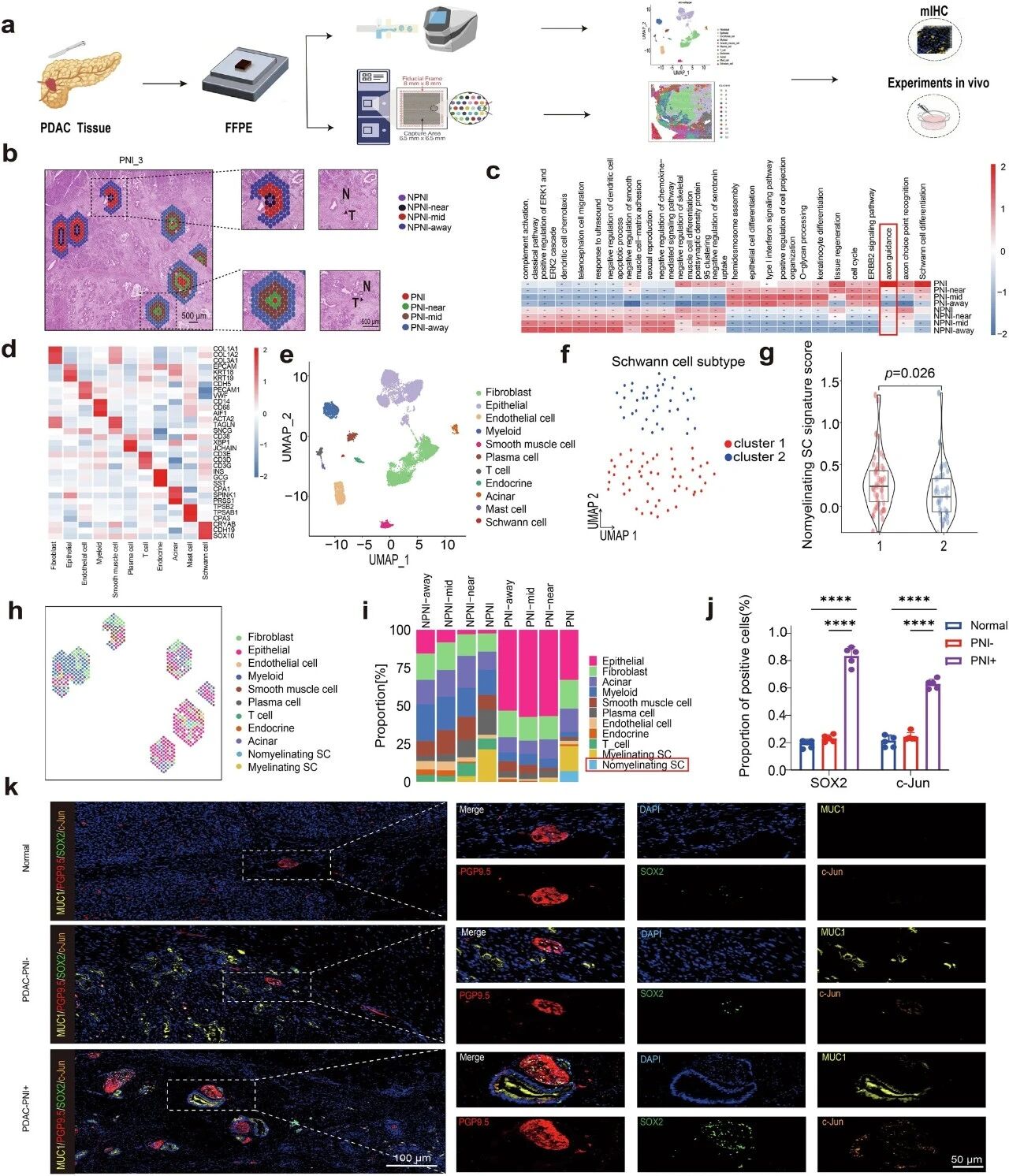
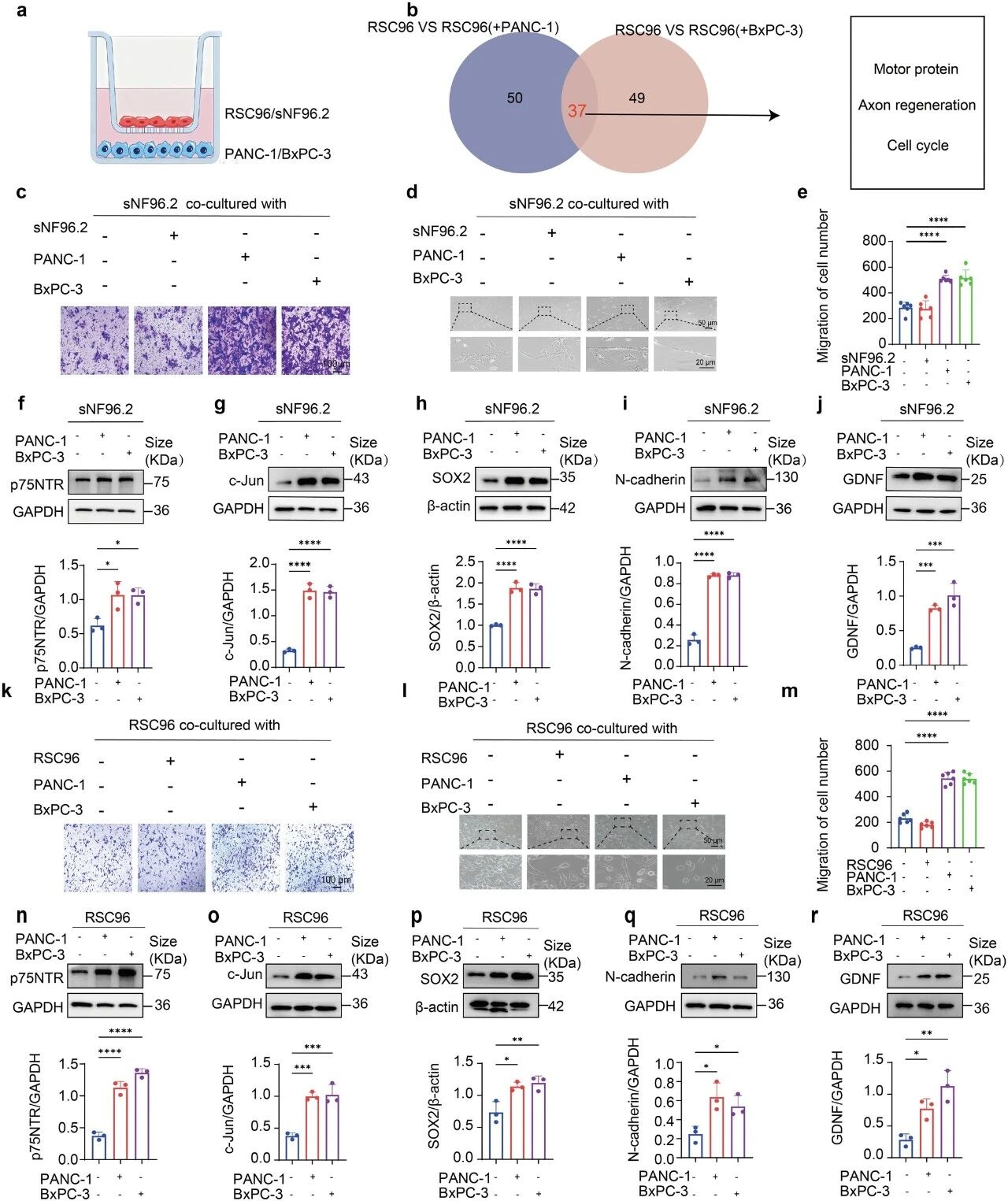
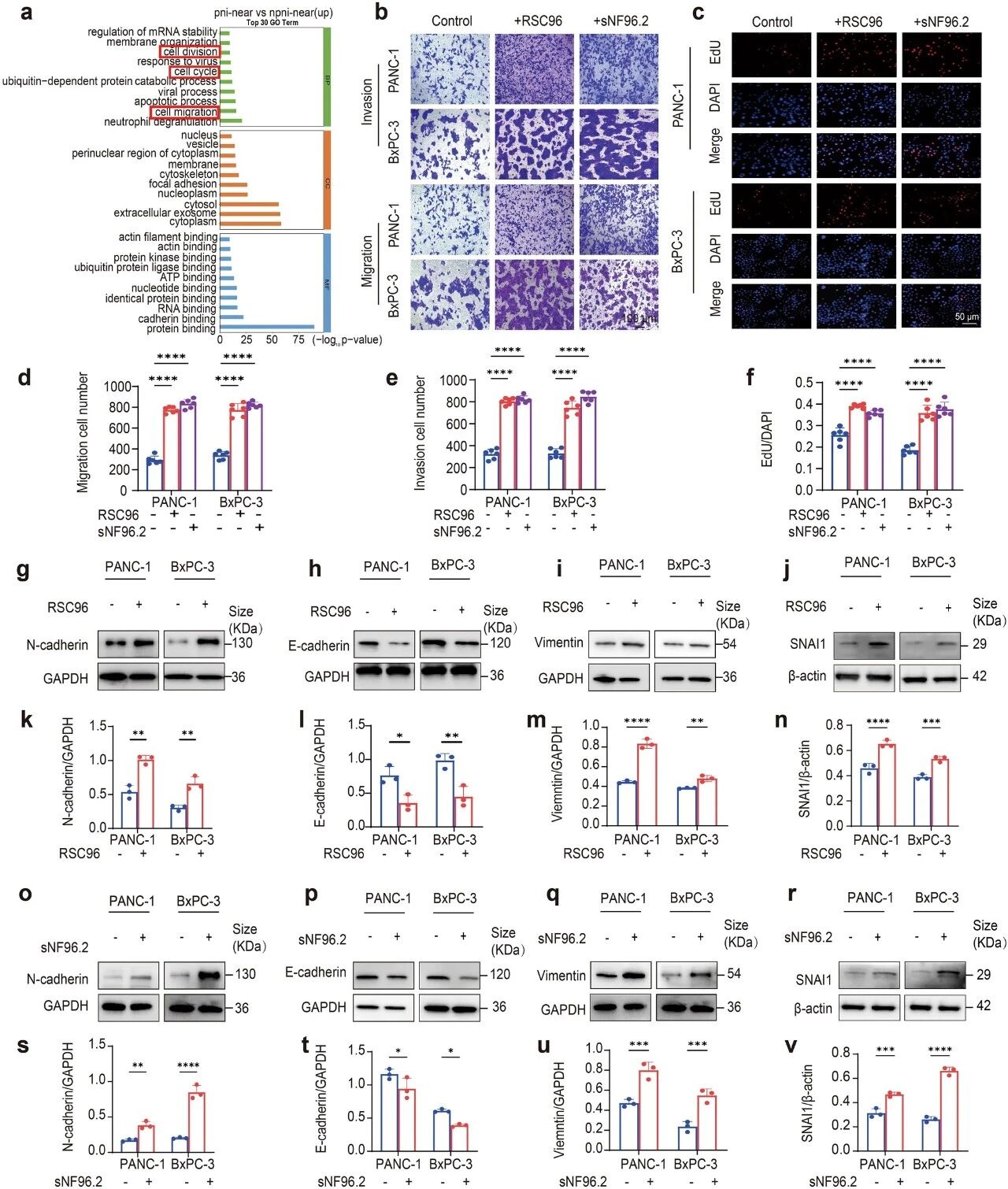
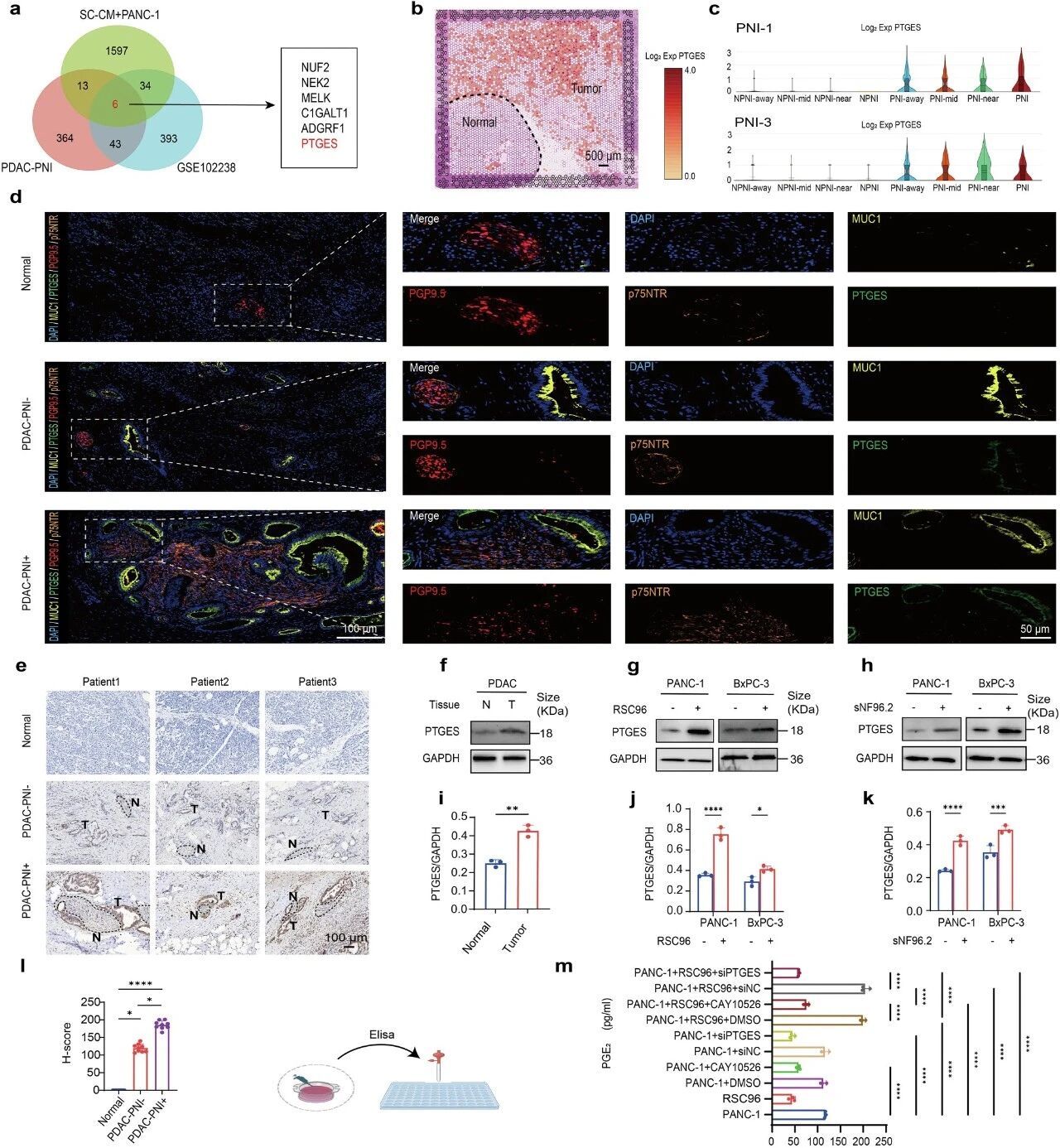
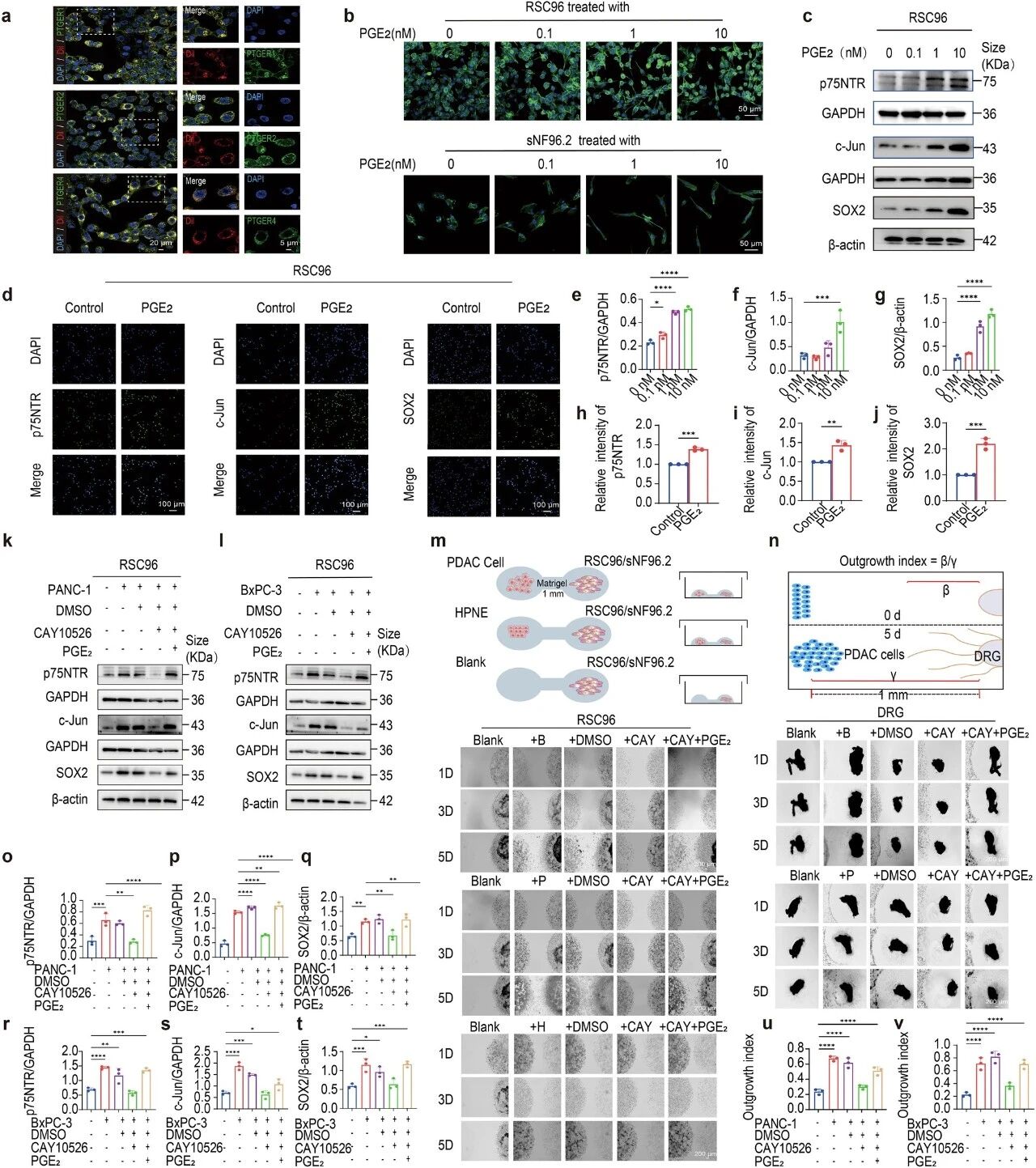
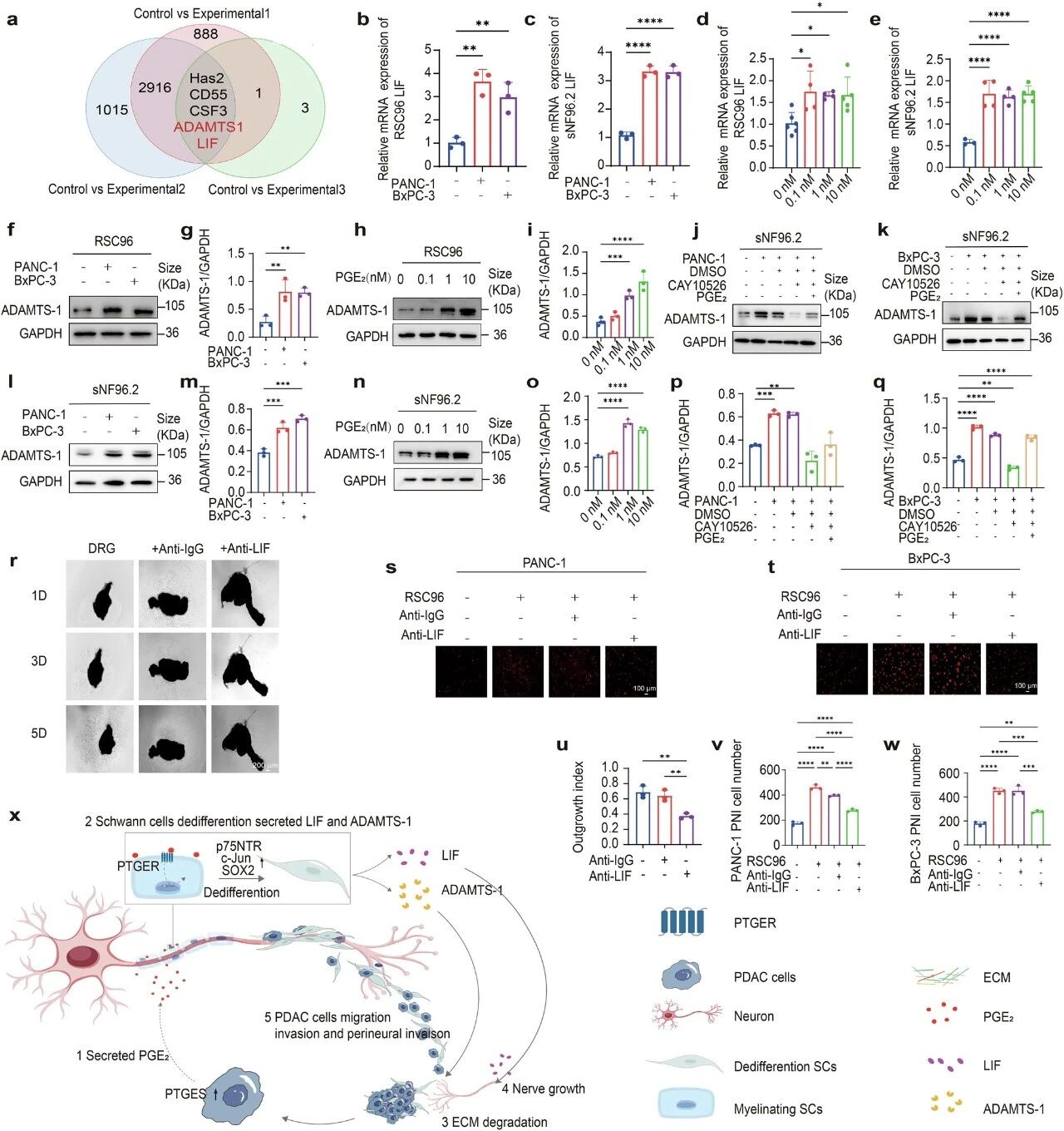
近日,清华大学董家鸿院士&福建医科大学郜峰/翁山耕/刘奇才团队在国际知名期刊《Signal Transduction and Targeted Therapy》发表一项关于胰腺导管腺癌(PDAC)神经浸润机制的重要研究。该研究首次系统阐明了肿瘤细胞如何“策反”神经周围的雪旺细胞,为其沿神经侵袭铺路的全新分子机制,并锁定了关键药物靶点。这一发现为改善胰腺癌这一“癌王”的预后带来了新的希望。 雪旺细胞在神经浸润阳性区域富集 临床困境:神经浸润——胰腺癌的致命“高速公路” 胰腺癌细胞促进雪旺细胞去分化 胰腺导管腺癌(PDAC)是恶性程度最高的实体肿瘤之一,患者五年生存率不足10%。其致命特性之一,便是高达70-100%的患者会出现“神经浸润”(PNI),即癌细胞沿着神经束扩散。神经浸润不仅是肿瘤局部复发和转移的“快车道”,更是导致患者剧烈疼痛和预后极差的核心因素。然而,长期以来,临床对神经浸润缺乏有效的预测方法和干预靶点,其起始机制一直是个谜。 核心发现:癌细胞“策反”雪旺细胞,共建侵袭桥梁 雪旺细胞诱导胰腺癌细胞恶性进展 研究通过整合临床样本的RNA测序、空间转录组学和单细胞分析,首次在神经浸润区域观察到一个显著现象:一类处于“去分化”状态的雪旺细胞(SCs)特异性富集。雪旺细胞是外周神经的主要胶质细胞,正常情况下负责营养和支持神经元。但在胰腺癌微环境中,它们被癌细胞重新编程,回到了类似神经损伤后的修复状态。 这就好比肿瘤细胞策反了神经的“守卫”雪旺细胞,让它们调转枪口,为肿瘤入侵神经“铺路搭桥”。这些去分化的雪旺细胞高表达p75NTR、SOX2、c-Jun等标志物,形态变为细长、具侵袭性,并展现出强大的迁移能力。 机制揭秘:PGE2是关键“信号兵”,驱动雪旺细胞叛变 共培养体系中PTGES/PGE2的升高与神经浸润相关 那么,肿瘤细胞发出的策反指令是什么?通过多组学数据交叉分析,研究团队将目光锁定在前列腺素E合成酶(PTGES)及其产物——前列腺素E2(PGE2)上。他们发现,在神经浸润区域的核心,肿瘤细胞高表达PTGES,其表达水平与患者PNI状态正相关。 随后的系列实验证实,胰腺癌细胞正是通过分泌PGE2,驱动了雪旺细胞的去分化。在共培养体系中,肿瘤细胞分泌的PGE2能诱导雪旺细胞形态改变,并显著上调其去分化标志物表达。当使用PTGES抑制剂、基因敲低或基因敲除手段阻断癌细胞产生PGE2后,雪旺细胞向肿瘤的定向迁移和神经突触生长能力被显著削弱。 被激活的雪旺细胞如何具体执行“铺路”任务?研究发现,在PGE2刺激下,去分化的雪旺细胞会大量分泌两种关键因子: 白血病抑制因子(LIF):一种多效性细胞因子,可促进神经重塑和神经元存活,为肿瘤细胞营造“亲神经”的微环境。 金属蛋白酶ADAMTS-1:能够降解神经周围的细胞外基质,物理上破坏神经束的屏障,为癌细胞浸润扫清障碍。 在三维共培养和动物模型中,使用LIF中和抗体或PTGES抑制剂,都能有效抑制肿瘤细胞的神经侵袭,并减轻模型动物的神经功能障碍和髓鞘损伤。 胰腺癌来源的PGE2诱导雪旺细胞活化 PGE2促进雪旺细胞分泌LIF和ADAMTS-1以驱动神经浸润发展 研究意义与未来展望 该研究革新了人们对神经侵润起始机制的认识:并非癌细胞先攻击神经,而是它们先“教化”了雪旺细胞,由后者主动创造利于侵袭的条件。这为我们干预胰腺癌神经浸润提供了两个极具潜力的新靶点:PTGES/PGE2轴和LIF。相较于传统靶向COX-2的药物可能带来的心血管和胃肠道副作用,直接靶向下游的PTGES可能更具安全性。同时,LIF本身也可作为治疗靶点或预测神经浸润的生物标志物。 原文链接: https://www.nature.com/articles/s41392-026-02648-x
声明:本文系药方舟转载内容,版权归原作者所有,转载目的在于传递更多信息,并不代表本平台观点。如涉及作品内容、版权和其它问题,请与本网站留言联系,我们将在第一时间删除内容